Sağlık Bakanlığı 22 Aralık'ta çocukluk çağında, yetişkinlerde ve yaralanma sonucu gebelere yapılan difteri tetanoz aşılarının 2. Sınıf B seviyesinde geri çekme işlemi uygulandığını bilmişti.
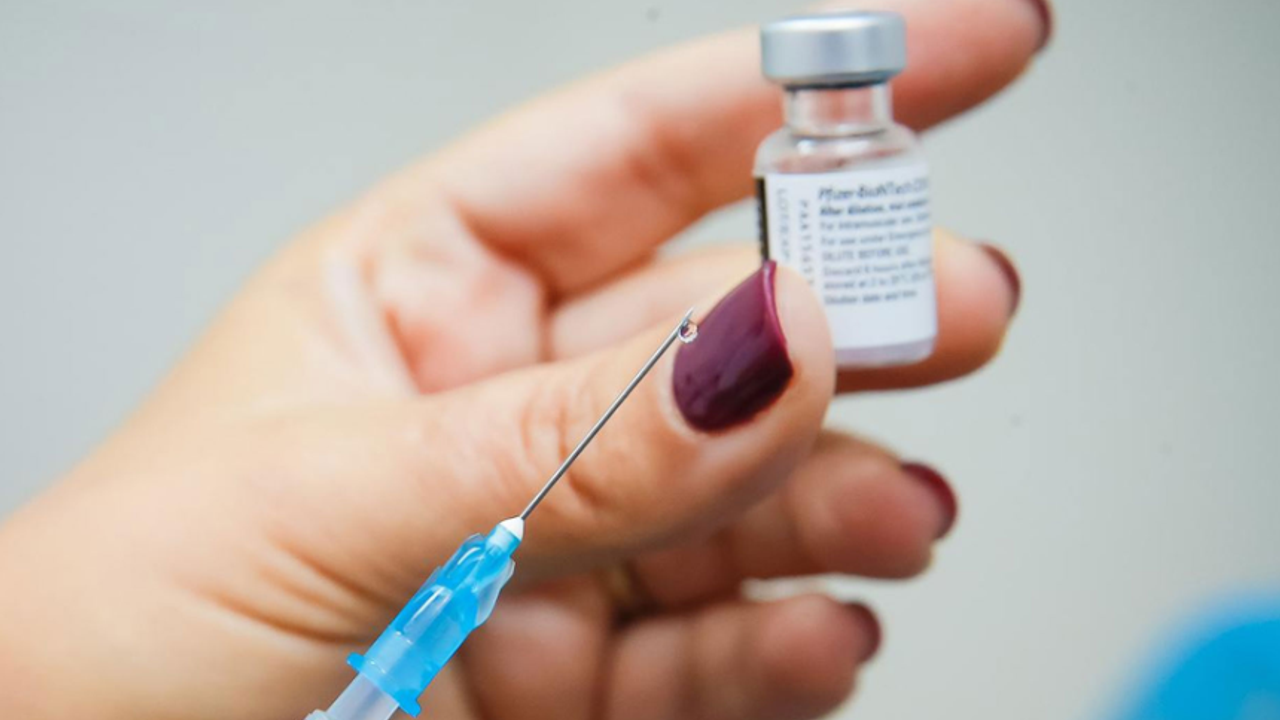
Sağlık Bakanlığı Türkiye İlaç ve Tıbbi Cihaz Kurumu'nun resmi sitesinden yapılan açıklamada, "Turk İlaç ve Serum San. A.Ş. üretim tesisi ile ilgili Kurumumuzun ilgili birimleri ve bilimsel komisyonlarınca yapılan inceleme ve değerlendirmeler neticesinde alınan karara istinaden “Tetadif 0,5 mL IM Enjeksiyonluk Süspansiyon” isimli ürünün halihazırda firma tarafından üretimi ve/veya dağıtımı yapılmış tüm serilerine 19 Kasım 2015 tarihli ve 29537 sayılı Resmi Gazete’de yayımlanan Geri Çekme Yönetmeliği’ne göre 2. Sınıf B seviyesinde (nihai kullanıcıya ürünü sağlayan tüm yerlere) geri çekme işlemi uygulanmış olup gereğinin yapılması ilgili paydaşlara duyurulmuştur. Tüm sağlık mesleği mensuplarına ve kamuoyuna önemle duyurulur" ifadeleri kullanıldı.
HALK SAĞLIĞI'NDAN AÇIKLAMA
Konuya ilişkin açıklama yapan Halk Sağlığı Genel Müdürlüğü ise "Bebekleri, çocukları ya da yetişkinleri, bir kısım enfeksiyon hastalıklarından korumanın en önemli ve en güvenli aracı aşılardır. Ülkemiz ise aşı ile önlenebilir hastalıklara karşı en kapsamlı, en etkin ve en güvenli bağışıklama programı uygulayan ülkelerin başında gelmektedir. Bu bağlamda bakanlığımız, tedarik ettiği aşıyı soğuk zincir şartlarını sağlayarak vatandaşımızın ulaşabileceği en uç noktaya gönderirken diğer taraftan aşı uygulamasıyla ortaya çıkabilecek en küçük yan etkiyi dahi hassasiyetle takip etmektedir" ifadesini kullandı.
'İLGİLİ SERİYE GERİ ÇEKME UYGULANDI'
Vatandaşın kullanımına sunulan her aşının Halk Sağlığı Genel Müdürlüğü'nün isteği ile Türkiye İlaç ve Tıbbi Cihaz Kurumu (TİTCK) ulusal referans laboratuvarlarında yeniden analiz edildiği belirtilerek, "Etkinliğinden ve güvenliğinden emin olunduktan sonra vatandaşımıza yapılana kadar Aşı Takip Sistemimiz tarafından takip edilmektedir. TİTCK tarafından geri çekme işlemi başlatılan 'Tetadif 0,5 ml IM Enjeksiyonluk Süspansiyon' isimli ürün, erişkinlere uygulanan tetanos-difteri aşısı olup, teknoloji transferi desteği sağlanarak ülkemizde ilk aşamadan itibaren üretilmeye başlanmış ilk aşıdır. Üretimin her süreci ulusal otorite olan TİTCK tarafından düzenli bir şekilde takip edilmektedir. Bahse konu aşının toplatılmasını gerektirecek istenmeyen etki bildiriminde bulunulmamıştır. Ancak son denetim esnasında eksiklik görülen bazı süreçlere bağlı olarak komisyon kararıyla ilgili seriye çekme uygulanmıştır. Yeni üretilen aşılar, özel şartlarda izlenerek raf ömürleri 3 yıla kadar peyderpey uzatılmaktadır. Söz konusu aşının raf ömrü de böyle bir sürecin sonunda 2 yıldan 3 yıla uzatılmıştır. Bu durum, söz konusu aşının miadının uzatılması işlemi değildir. Gerekli kontrolleri yapılmış, kullanıma uygun, yeterli miktarda aşı stoğumuz mevcuttur. Bu açıdan herhangi bir sıkıntı yaşanması söz konusu değildir" ifadelerine yer verildi.(DHA)